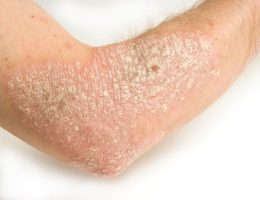
מנהל המזון והתרופות האמריקאי (ה-FDA) אישר את bimekizumab (BIMZELX) לטיפול בפסוריאזיס פלאק בינוני עד חמור במבוגרים המועמדים לטיפול סיסטמי או לפוטותרפיה. Bimekizumab הוא הטיפול היחיד המאושר לטיפול בפסוריאזיס שמעכב באופן סלקטיבי את שני הציטוקינים אינטרלוקין 17A ואינטרלוקין 17F.
האישור של התרופה התבסס על נתונים משלושה מחקרי פאזה 3, מחקרים רב-מרכזיים ואקראיים (BE READY, BE VIVID ו-BE SURE), אשר העריכו את היעילות והבטיחות של bimekizumab ב-1,480 מבוגרים עם פסוריאזיס פלאק בינוני עד חמור.
לפי הודעת החברה, “אישור ה-FDA של BIMZELX הוא אבן דרך מרגשת המשקפת את המחויבות שלנו לשיפור מתמיד בסטנדרט הטיפול בפסוריאזיס פלאק. בניסויי פאזה 3 שלנו, בשבוע ה-16, 85-91% מהחולים שטופלו ב-bimekizumab הגיעו לתוצא של עור נקי או כמעט נקי, ו-59-68% מהמטופלים הגיעו לתוצא של עור נקי. לאחר ש-bimekizumab אושר לפסוריאזיס, אנו נתקדם להגשת בקשות להתוויות נוספות בארה”ב”.
עוד היא נכתב בהודעת החברה כי “בניסויים, bimekizumab השיג רמות גבוהות יותר של עור נקי בשבוע 16 בהשוואה לפלסבו ושלוש תרופות ביולוגיות קיימות לפסוריאזיס, כאשר התגובות היו מהירות ונמשכו עד לשנה. נתונים ארוכי טווח הראו גם שרוב החולים שמרו על רמות גבוהות של תגובה קלינית במשך שלוש שנים”.














השאירו תגובה
רוצה להצטרף לדיון?תרגישו חופשי לתרום!