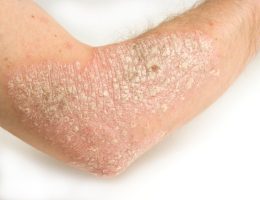
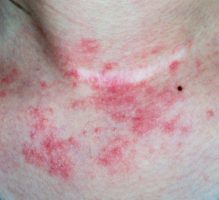
מנהל המזון והתרופות האמריקאי (Food and Drug Administration) אישר את מתן קרם Tapinarof (Vtama) לטיפול בחולים עם פסוריאזיס רובדי בדרגה קלה, בינונית, או חמורה.
המומחים מסבירים כי Tapinarof, אגוניסט לקולטן ל-Aryl Hydrocarbon, הינו הטיפול המקומי הראשון המאושר לטיפול בפסוריאזיס מזה למעלה מ-25 שנים ומהווה את התרופה היחידה שאינה-סטרואידים המאושרת להתוויה זו.
אישור הטיפול מבוסס על נתונים משני מחקרים בשלב 3, PSOARING 1 ו-PSOARING 2, כמו גם ממחקר הארכה ארוך-טווח PSOARING 3.
שיפור מובהק סטטיסטי במדד PGA (Psoriasis Global Assessment) של נקי או כמעט-נקי, עם שיפור של לפחות שתי דרגות לאחר 12 שבועות תועד ב-36% מהחולים שטופלו ב- Tapinarof במחקר PSOARING 1 וב-40% מאלו שטופלו במחקר PSOARING 2, בהשוואה ל-6% בלבד בכל קבוצת ביקורת.
במחקר הארכה בתווית-פתוחה, 40% מהחולים שהשיגו מדד PGA של 0/1 במהלך המחקרים הראשוניים הדגימו השפעה ממושכת ללא טיפול לאורך חציון של ארבעה חודשים.
המומחים מאמינים כי לטיפול המאושר החדש צפוי מקום משמעותי במכלול אפשרויות הטיפול בחולים עם פסוריאזיס.
מתוך הודעת ה-FDA

















השאירו תגובה
רוצה להצטרף לדיון?תרגישו חופשי לתרום!