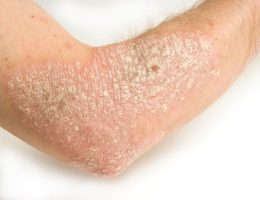
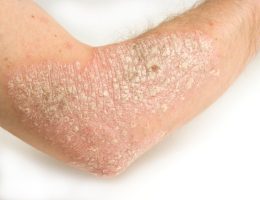
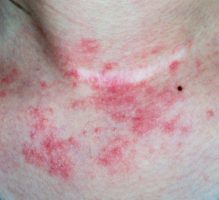
ועידת CHMP (Committee for Medicinal Products for Human Use) מטעם ה-EMA (European Medicines Agency) המליצה על אישור הטיפול ב- Guselkumab כנגד פסוריאזיס רובדית.
הועדה תמכה במתן הטיפול במבוגרים עם פסוריאזיס רובדית בדרגה מתונה-עד-חמורה, שהם מועמדים לטיפול סיסטמי, לאחר שהעדויות העידו כי לטיפול יעלות משמעותית וממושכת בחולים אלו.
הפאנל האירופי קבע את ההמלצה על-בסיס נתוני מחקרי VOYAGE 1 ו-VOYAGE 2, שהראו כי Guselkumab עדיף על Adalimumab (יומירה) ונתונים נספים ממחקר NAVIGATE, בו חולים החליפו מ-Ustekinumab (סטלרה) ל- Guselkumab.
הצפי בחברה הוא לקבל את האישור הסופי בסוף שנת 2017. Guselkumab כבר משווק בארצות הברית, לאחר שאושר ע”י מנהל המזון והתרופות האמריקאי ביולי לטיפול במבוגרים עם פסוריאזיס רובדית בדרגה מתונה-עד-חמורה, שהם מועמדים לטיפול סיסטמי או פוטותרפיה.
מתוך הודעת ה-EMA
















השאירו תגובה
רוצה להצטרף לדיון?תרגישו חופשי לתרום!