חברת Abbott Laboratories Inc זכתה בתמיכת פאנל מומחים בארצות הברית לשימוש רחב יותר בתרופה Humira (Adalimumab) לטיפול בחולים עם Ulcerative Colitis.
פאנל של יועצים מחוץ למנהל התרופות והמזון האמריקאי הצביעו ברוב של 15 לעומת 2 לשאלה האם התועלת של Humira עולה על הסיכונים הכרוכים בטיפול בחולים עם Ulcerative Colitis.
מנהל התרופות והמזון האמריקאי לרוב עוקב אחר המלצות הפאנל, אם כי אינו נדרש לעשות כן. החלטה סופית בנושא צפויה בסוף השנה.
בחברת התרופות מקווים להרחיב את השימוש ב-Humira לחולים עם Ulcerative Colitis בינוני עד חמור, ששכיחותה עומדת על כ-700,000 חולים בארצות הברית. התרופה תשמש רק בחולים בהם נכשל טיפול תרופתי אחר למחלה.
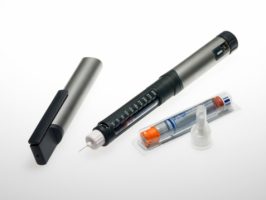
במידה והתרופה תאושר לטיפול בחולים אלו, אזי Humira צפויה להיות התרופה הביולוגית הראשונה אותה חולים יכולים להזריק לעצמם. Remicade, תרופה מתחרה העובדת במנגנון דומה ל-Humira, ניתנת כטיפול תוך-ורידי.
עם זאת, מרבית חברי הפאנל קראו לחברת התרופות לערוך מחקרים נוספים לאחר אישור התרופה, בעיקר במטרה לבחון אם התרופה מומלצת במינון גבוה יותר.
לציין כי מנהל התרופות והמזון האמריקאי דחה את הבקשה הראשונה של חברת התרופה לאישור Humira לטיפול ב-Ulcerative Colitis בנובמבר האחרון, בטענה כי התוצאות ממחקרים קליניים אינם מוכיחים באופן חד-משמעי כי התרופה סייעה בעצירת תסמיני המחלה, הכוללים שלשולים, דימום רקטאלי, אי-נקיטת שתן, כאבי בטן, חום, עייפות וירידה במשקל.
חלק מהיועצים החיוניים גם הטילו ספק בשאלה אם הבדל של פחות מ-10% בין Humira ופלסבו הינו הבדל בעל משמעות, על-בסיס נתונים ממחקרים קליניים. אך אחרים טענו כי גם תועלת צנועה עשויה לסייע לאלו עם מעט מאוד אפשרויות.















השאירו תגובה
רוצה להצטרף לדיון?תרגישו חופשי לתרום!